近日,环化学院纳米所苏倩倩副研究员团队及其合作者在国际高水平期刊《Advanced Materials》(影响因子:30.849)上发表题为“Deciphering nanoparticle trafficking into glioblastomas uncovers an augmented antitumor effect of metronomic chemotherapy”的研究论文。
纳米颗粒在治疗胶质母细胞瘤(GBM)的研究中得到了广泛的关注,因为它们可以穿过血脑屏障(Blood-brain barrier, BBB),选择性地靶向GBM细胞,并能够在肿瘤部位延长药物释放时间。这些属性赋予了纳米颗粒作为多功能载体,揭示治疗GBM复杂机制和相关反应的巨大潜力。尽管之前国际上已经有大量的研究展示此方面工作,但目前还没有关于纳米颗粒能否进入GBM细胞及其定位的直接证据。除此之外,在静脉给药后,纳米颗粒进入GBM细胞及其对治疗GBM的复杂机制作用还缺乏深入理解。我校环境与化学工程学院纳米所苏倩倩副研究员联合团队,设计制备了具有靶向功能的稀土纳米药物载体,基于颅内胶质母细胞瘤模型,首次利用透射电子显微镜证明纳米颗粒可以穿过BBB,内吞到胶质母细胞瘤U87-MG细胞的溶酶体中,并在光化学电离时实现从内涵体/溶酶体逃逸。此外,利用双载药纳米体系,验证了纳米药物低剂量多次(MetNano)的给药策略能产生更优的抗肿瘤治疗效果。这项研究为胶质母细胞瘤和其他晚期实体瘤的安全有效治疗提供了新的策略,对于促进治疗GBM的纳米药物临床转化至关重要。
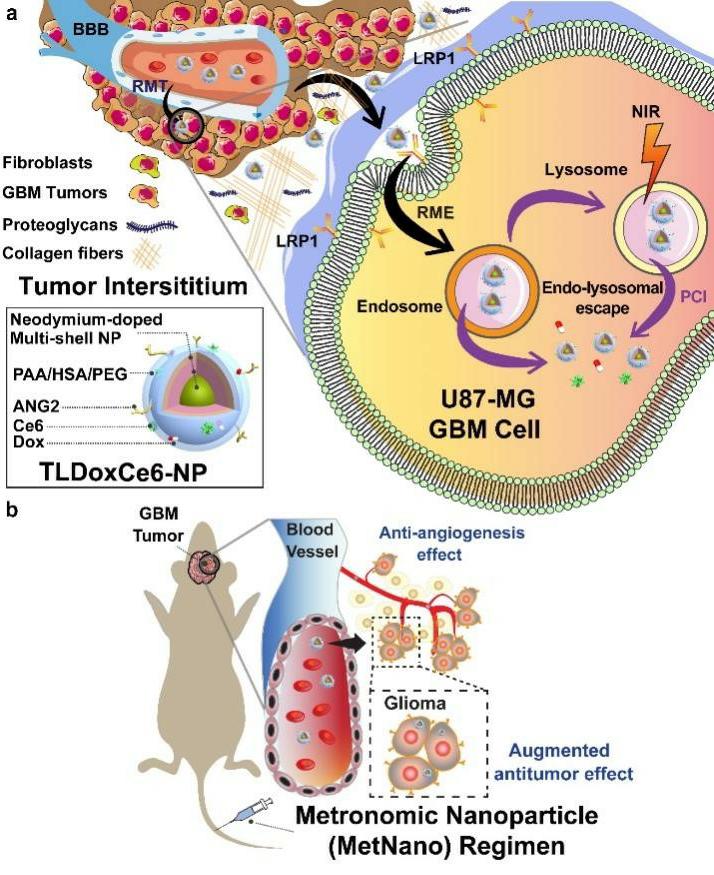
图1 基于MetNano给药策略,纳米颗粒穿过BBB,进入胶质瘤细胞促进抗肿瘤血管生成治疗和增强抗肿瘤作用的示意图。
该工作由亚星221net、新加坡国立大学等合作完成,苏倩倩副研究员为通讯作者,并得到了科技部国家重点研发计划和国家自然科学基金青年基金等资助和支持。
文章链接:https://onlinelibrary.wiley.com/doi/abs/10.1002/adma.202106194
